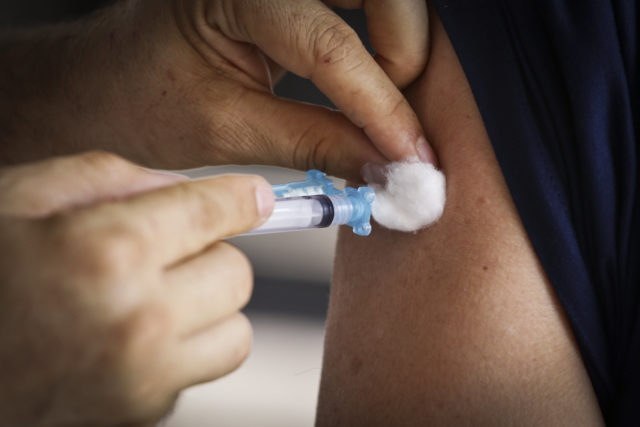
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou recentemente os testes clínicos no Brasil de uma nova vacina contra a Covid-19, desenvolvida pela farmacêutica Sanofi Pasteur. Ao todo, serão testados 150 voluntários brasileiros nos estados da Bahia, Minas Gerais, Mato Grosso do Sul e Rio de Janeiro.
Além da Sanofi Pasteur, outras oito vacinas estão sendo testadas em voluntários brasileiros, com autorização da Anvisa: Butanvac (Butantan); Chadox 1 NCOV19; Coronavac (Butantan); Clover; Covaxin (Precisa); Jassen Vaccine; Medicago e Comirnaty (Pfizer). Os detalhes estão disponíveis no link.
Em nota, a Anvisa informa que “a autorização de uma pesquisa clínica está baseada em dois pontos centrais: a segurança para os voluntários da pesquisa e a capacidade do desenho do estudo em produzir dados confiáveis e verificáveis. Para análise de um estudo clínico, a Anvisa se baseia nos dados pré-clínicos e em outras informações disponíveis sobre a vacina candidata”.
“Após a autorização, o laboratório pode iniciar a vacinação dos voluntários. Os centros participantes da pesquisa são responsáveis pelo monitoramento destes voluntários e pelo relato dos eventos adversos ocorridos durante a pesquisa. Os eventos adversos graves devem ser notificados de forma imediata para a Anvisa. Outros eventos devem ser relatados nos relatórios de pesquisa”.
Ainda de acordo com a Anvisa, “o tempo de duração dos estudos depende diretamente dos laboratórios e de fatores inerentes ao próprio processo de pesquisa. Das nove vacinas em testes no Brasil, quatro ainda não solicitaram autorização de uso emergencial ou registro no país: Clover, Medicago, Covaxin e Sanofi Pasteur”.
Passo a passo dos testes
A infectologista e especialista em vacinas do Exame Imagem e Laboratório/Dasa, Maria Isabel de Moraes Pinto, explica que antes de iniciar os testes em seres humanos, os laboratórios devem realizar os testes pré-clínicos em células, para detectar os antígenos mais importantes (do vírus ou da bactéria) que serão utilizados nas vacinas. Em seguida, é necessário realizar os testes em animais e, preferencialmente, publicar os resultados.
Assim que a vacina se mostrar segura para aplicação em humanos, iniciam-se os testes clínicos, que são divididos em três fases.
“Na fase um, testa-se a segurança da vacina em um número pequeno de indivíduos sadios. Na fase dois, passa-se a avaliar diferentes doses da vacina, continua-se avaliando a segurança e também a capacidade dessa vacina de produzir anticorpos e células que possam ser importantes na resposta à vacinação. E, se a fase dois tem bom resultado, passa-se para a fase três, em que se avalia a eficácia da vacina”, explica Maria Isabel de Moraes.
De acordo com o infectologista do Hospital Anchieta de Brasília, Victor Bertollo, na fase dois, o número de voluntários aumenta e passa a contemplar pessoas do grupo alvo da imunização, como crianças, idosos ou população em geral, e não apenas indivíduos sadios.
A especialista em vacinas Maria Isabel de Moraes explica que, na fase três, os pesquisadores selecionam um grupo de controle que não é vacinado (ou é vacinado com um imunizante completamente diferente) e um grupo que recebe a dose da vacina a ser testada. Em seguida, eles observam os resultados para descobrir qual é a capacidade da vacina de diminuir os casos de determinada doença no grupo vacinado, em comparação com aqueles que não receberam o imunizante.
A infectologista Maria Isabel de Moraes esclarece que os laboratórios precisam apresentar atestados e evidências de boas práticas para que tenham autorização da Anvisa para realizar os testes clínicos das vacinas.
“Se é uma vacina inativada, tem que mostrar como aconteceu o processo de inativação; se é uma vacina com vírus vivo atenuado, tem que mostrar como isso é feito e provar que realmente esses testes são feitos de maneira adequada. Se tratar de ensaios de fase três mais adiantados, tem que mostrar os resultados de fase um e dois e também os resultados de testes pré-clínicos.”
De acordo com a especialista, esse passo a passo dos testes clínicos é válido para todas as vacinas. “Na situação de pandemia, temos utilizado muitas vezes um ensaio de fase 1/2, ou seja, testamos a segurança, mas também testamos diferentes doses de vacina, enquanto vemos a produção de anticorpos. Sempre de maneira mais ágil, mas não perdendo a capacidade de avaliar adequadamente essa vacina”, acrescenta.
O infectologista Victor Bertollo ressalta que as fases um e dois dos testes clínicos não precisam ser realizadas necessariamente no Brasil. Mas o laboratório precisa apresentar os resultados, caso queira iniciar os testes da fase três com voluntários brasileiros.
Efeitos Adversos
Segundo o infectologista Victor Bertollo, os eventos adversos são monitorados ao longo de todas as etapas. “Na fase um e dois, consegue-se identificar, principalmente, os eventos comuns e muito comuns, que são dor no local da aplicação, mal-estar, febre, algumas reações inespecíficas autolimitadas”, explica.
Nos casos de efeitos adversos graves, ocasionados principalmente na fase três – quando o número de voluntários é maior -, a Anvisa deve ser comunicada imediatamente para que o caso seja avaliado.
“Pode ocorrer alguns eventos graves, não necessariamente causados pela vacina. Também é necessário ter um comitê externo à pesquisa, para que ele possa realmente fazer uma análise isenta do evento e dizer se o estudo poderá dar seguimento ou não.”
“Primeiro: fazer o desenho do caso; ver se era, por exemplo, do grupo que estava sendo vacinado ou se era do grupo placebo. E segundo: fazer uma análise do evento adverso, para ver se existe uma possível relação de causa e efeito, ou seja, se é possível que essa vacina, que está sendo testada, possa ter sido a causa do evento adverso.”
Vacinômetro
Dados do Ministério da Saúde mostram que 83.989.928 brasileiros tomaram a primeira dose de alguma vacina contra a Covid-19 (40% da população do país) e 30.607.941 já tomaram a dose de reforço (14,5%).
Ao todo, já foram distribuídas 147.335.318 doses de imunizantes contra o coronavírus aos estados brasileiros. Os dados são da manhã desta segunda-feira (12).
