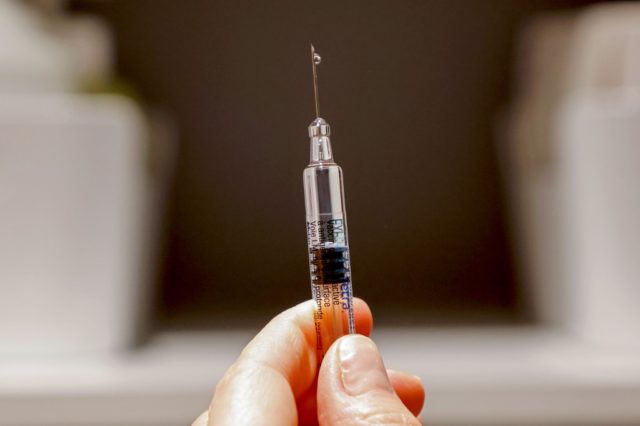
A pharmacist vaccinates a patient against the seasonnal flu at a pharmacy in Paris on october 13, 2020. (Photo by Ludovic MARIN / AFP)
O voluntário brasileiro que participava dos estudos da vacina contra o coronavírus em desenvolvimento pela Universidade de Oxford (Reino Unido) morreu por complicações da Covid-19 e não recebeu a imunização em teste. A informação foi confirmada à reportagem por fontes ligadas ao governo britânico, em Londres, e que acompanham os testes.Em nota divulgada nesta quarta (21), a Anvisa (Agência Nacional de Vigilância Sanitária) confirmou ter sido comunicada sobre a morte do voluntário, mas não deu detalhes do caso.
A agência, porém, disse ter recebido dados de um comitê internacional de avaliação de segurança que recomendou a continuidade dos estudos, sem prejuízos à segurança, o que já sugeria que o voluntário fizesse parte do chamado grupo controle, que recebe outro medicamento, imunização ou substância placebo, sem efeito nenhum, para comparação de eficácia e efeitos colaterais.
No caso do teste da vacina de Oxford, os voluntários recebem a vacina contra a Covid-19 ou a vacina meningocócica.
“É importante ressaltar que, com base nos compromissos de confidencialidade ética previstos no protocolo, as agências reguladoras envolvidas recebem dados parciais referentes à investigação realizada por esse comitê, que sugeriu pelo prosseguimento do estudo. Assim, o processo permanece em avaliação”, informou a Anvisa.
Em nota, a Astrazeneca Brasil informou que não poderia comentar casos individuais por questões de confidencialidade, mas diz que “todos os processos de revisão exigidos foram seguidos”.
“Todos os eventos médicos significativos são avaliados cuidadosamente pelos investigadores do estudo, um comitê independente de monitoramento de segurança e autoridades regulatórias. Essas avaliações não levaram a quaisquer preocupações sobre a continuidade do estudo em andamento”, disse a empresa, em nota.
A Universidade de Oxford, por sua vez, informou que incidentes significativos entre participantes do grupo controle ou do braço de intervenção são revisados independentemente. “Após avaliação cuidadosa deste caso no Brasil, não houve preocupações sobre a segurança do ensaio clínico e a revisão independente, além do regulador brasileiro, recomendou que o ensaio deveria continuar”, informou a universidade.
A vacina de Oxford está na chamada fase 3, que é a última etapa antes da aprovação, na qual são confirmados dados prévios de segurança e também de eficácia em um número maior de voluntários. Os testes foram iniciados em junho com profissionais de saúde, por seu alto risco de contrair o coronavírus, e ocorrem em São Paulo, Salvador, Rio de Janeiro, Rio Grande do Norte e Rio Grande do Sul.
Em setembro, a AstraZeneca chegou a informar uma pausa nos testes após a suspeita de uma possível reação adversa grave em uma participante do Reino Unido. Após avaliação de um comitê independente de segurança, os testes foram retomados.
A Anvisa afirmou na época que, “após avaliar os dados do evento adverso, sua causalidade e o conjunto de dados de segurança gerados no estudo, a agência concluiu que a relação benefício/risco se mantém favorável”. Assim, os testes continuaram a ser feitos também no Brasil.
Os estudos no país são coordenados pela Unifesp (Universidade Federal de São Paulo). Em nota divulgada na quarta-feira, a universidade disse que se solidariza com a família do voluntário que morreu e que não houve registro de intercorrências graves ligadas à vacina.
“Até o momento, 8.000 voluntários já foram recrutados e receberam uma ou já as duas doses indicadas no estudo. Tudo avança como o esperado, sem ter havido qualquer registro de intercorrências graves relacionadas a vacina envolvendo qualquer um dos voluntários participantes”, informou.
Folhapress
